
- 7 آذر 1400
- 4 نظر
اسید فسفریک چیست ؟
List of Contents
اسید فسفریک ( در لفظ انگلیسی : phosphoric acid ) که ارتوفسفریک اسید (H 3 PO 4 ) نیز نامیده می شود ، مهم ترین اسید اکسیژن از فسفر می باشد که برای تبدیل فسفات نمک به کود استفاده می شود . همچنین در دندانپزشکی، در تهیه مشتقات آلبومین و در صنایع قند و نساجی نیز کاربرد دارد . اسید فسفریک به عنوان طعم دهنده اسیدی و میوه مانند در محصولات غذایی عمل می کند.
اسید فسفریک خالص به صورت یک جامد کریستالی با نقطه ذوب ۴۲.۳۵ درجه سانتیگراد یا ۱۰۸.۲ درجه فارنهایت می باشد. در شکل مایع به صورت بیرنگ و شربتی است . اسید فسفریک خام از سنگ فسفات تهیه می شود ، در حالی که اسید فسفریک با خلوص بالاتر از فسفر سفید ساخته می شود.
اسید فسفریک سه کلاس نمک را تشکیل می دهد که مربوط به جایگزینی یک، دو یا سه اتم هیدروژن است. از جمله نمک های فسفات مهم عبارتند از:
- سدیم دی هیدروژن فسفات (NaH 2 PO 4 ) که برای کنترل غلظت یون هیدروژن (اسیدیته) محلول ها استفاده می شود.
- دی سدیم هیدروژن فسفات (Na 2 HPO 4 ) که در تصفیه آب به عنوان رسوب دهنده برای کاتیون های فلزی با بار زیاد استفاده می شود.
- تری سدیم فسفات (Na 3 PO 4 ) که در صابون ها و مواد شوینده استفاده می شود.
- کلسیم دی هیدروژن فسفات یا سوپر فسفات کلسیم (Ca[H 2 PO 4 ] 2 ) که عمده مواد تشکیل دهنده کود می باشد.
- کلسیم مونوهیدروژن فسفات (CaHPO 4 ) که به عنوان یک عامل تهویه برای نمک ها و قندها استفاده می شود.
مولکول های اسید فسفریک تحت شرایط مناسب، اغلب در دماهای بالا، برای تشکیل مولکول های بزرگتر (معمولاً با از دست دادن آب) برهم کنش می کنند. بنابراین، اسید دی فسفریک یا پیروفسفریک (H 4 P 2 O 7 ) از دو مولکول اسید فسفریک، کمتر از یک مولکول آب تشکیل می شود .
این سادهترین سری مولکولهای همولوگ زنجیره بلند به نام اسیدهای پلی فسفریک است، با فرمول کلی H(HPO 3 ) n OH، که در آن n = 2، 3، 4، . . . . اسیدهای متافسفریک، (HPO 3 ) n ، که در آن n= 3، 4، 5، . . .، دسته دیگری از اسیدهای فسفریک پلیمری هستند.
اسیدهای متافسفریک شناخته شده با ساختارهای مولکولی حلقوی مشخص می شوند. اصطلاح متافسفریک اسید همچنین برای اشاره به یک ماده چسبناک و چسبناک که مخلوطی از هر دو شکل زنجیره بلند و حلقه ای (HPO 3 ) n است، استفاده می شود . اشکال مختلف پلیمری اسید فسفریک نیز با هیدراتاسیون اکسیدهای فسفر تهیه می شوند.
ویژگی های اسید فسفریک
| فرمول مولکولی | H3PO4 or H3O4P |
| جرم مولی | 97.995 g/mol |
| چگالی | 1.9 g/cm³ |
| نقطه ذوب | 42.4 °C |
| نقطه جوش | 407 °C |
| شکل ظاهری | مایعی غلیظ بدون رنگ و بو |
| حلالیت در آب | 548g در 100 گرم آب در دمای 20 °C |
| اسیدیته | 1.5 |
کاربردهای اسید فسفریک
کاربرد اسید فسفریک در کشاورزی:

در کشاورزی بیشتر اسید فسفریک تولید شده برای تولید کود استفاده می شود. عمدتاً به سه نمک فسفات تبدیل می شود که به عنوان کود استفاده می شود. که به شرح زیر است:
- سوپر فسفات سه گانه (TSP)
- دی آمونیوم هیدروژن فسفات (DAP)
- مونو آمونیوم دی هیدروژن فسفات (MAP)
اسید فسفریک همچنین در مکمل در خوراکی که به گاو، خوک و طیور داده می شود استفاده می شود.
افزودنی های مواد غذایی:
محلول های رقیق اسید فسفریک طعم اسیدی دلپذیری دارند. از این رو از آن به عنوان افزودنی غذایی استفاده می شود.این اسید به این موارد خاصیت اسیدی می دهد:
- نوشابه های گازدار
- سایر غذاهای آماده
- محصولات تصفیه آب
کاربرد اسید فسفریک در ساخت:
- ژلاتین.
- تثبیت کننده خاک
- واکس و جلا می دهد
- چسب برای سرامیک
- کربن فعال
- در دریاچه ها در رنگرزی پنبه
کاربرد اسید فسفریک در پزشکی:
- در سیمان دندان.
- برای تهیه مشتقات آلبومین.
- برای اسیدی کردن ادرار.
- برای از بین بردن بقایای نکروزه (سلول های مرده یا بافت).
- در داروهای ضد تهوع .
- در سفید کننده های دندان و مایع دهان شویه.
کاربرد اسید فسفریک در مراقبت شخصی :
این ماده برای طیف وسیعی از محصولات مراقبت شخصی ضروری است، از جمله:
- محصولات پاک کننده
- محصولات حمام
- عطرها
- محصولات مراقبت از مو
- محصولات ناخن
- آرایش
- محصولات مراقبت از پوست
- برای کنترل PH این محصولات نیز از اسید فسفریک استفاده می شود.
کاربرد اسید فسفریک در زدودن زنگ:
این اسید معمولاً برای زدودن زنگ استفاده می شود. این ماده هنگامی که روی زنگ زده می شود، با زنگ فلزاتی مانند فولاد و آهن واکنش نشان می دهد. بعد، زنگ را به یک ترکیب سیاه رنگ به راحتی قابل جابجایی تبدیل می کند.
سایر کاربردهای اسید فسفریک عبارتند از:
- محصولات مراقبت از خودرو
- باتری ها
- پاک کننده های صنایع نیمه هادی
- تمیز کردن و تجهیز محصولات مراقبتی
- محصولات برقی و الکترونیکی
- بسته بندی غذا
- سوخت و محصولات مرتبط
- محصولات لباسشویی و ظرفشویی
- محصولات مراقبت از چمن و باغ
- محصولات فلزی که در جای دیگر پوشش داده نشده اند
- رنگ و پوشش
- محصولات کاغذی
- لوازم عکاسی، فیلم و مواد شیمیایی عکس
- محصولات پلاستیکی و لاستیکی که در جای دیگری پوشش داده نشده اند
- فروش مجدد
- توزیع شیمیایی
- محیط های تخمیر صنعتی
- پاک کننده ها در فرآیندهای آبکاری برای خودرو و ماشین آلات
خطرات اسید فسفریک
اسید فسفریک ممکن است اثرات حاد یا مزمن سلامتی ایجاد کند. اثرات حاد سلامتی ممکن است بلافاصله یا اندکی پس از قرار گرفتن در معرض اسید فسفریک رخ دهد:
- تماس با چشم می تواند باعث تحریک و سوزش چشم شود.
- تنفس اسید فسفریک می تواند بینی و گلو را تحریک کرده و باعث سرفه و خس خس سینه شود .
اثرات طولانی مدت یا مزمن عبارتند از:
- ریه ها را تحریک می کند و باعث برونشیت می شود
- خشک شدن و ترک خوردن پوست
درمان مسمومیت با اسید فسفریک
اگر در معرض اسید فسفریک قرار گرفتید، می توانید قبل از درخواست کمک پزشکی، برخی از دستورالعمل های کمک های اولیه را دنبال کنید.
چنانچه این اسید با پوست و چشم ما تماس داشت,بلافاصله چشم و یا پوست خود را با مقدار زیادی آب حداقل به مدت ۳۰ دقیقه شستشو دهید.
در صورت نوشیدن اسید فسفریک، دهان خود را با آب بشویید. اگر شروع به استفراغ کردید، شستشو را متوقف کنید و برای کاهش خطر آسپیراسیون (ورود تصادفی مایعات یا جامدات به مجرای تنفسی ) به جلو خم شوید . سپس شستشوی دهان را با آب از سر بگیرید.
اگر این ماده شیمیایی را تنفس کردید، فوراً بروید و هوای تازه استنشاق کنید .
تولید اسید فسفریک
این ماده طی دو فرآیند ساخته می شود:
- فرآیند مرطوب
- فرآیند حرارتی
روش حرارتی معمولاً محصول غلیظتر و خالصتری تولید میکند، اما انرژی بر است (به دلیل تولید خود فسفر. اسید تولید شده از مسیر مرطوب خلوص کمتری دارد اما در ساخت کودها استفاده میشود).
(الف) فرآیند مرطوب
اسید فسفریک از فلوراپاتیت، معروف به سنگ فسفات، 3Ca3(PO4)2.CaF2، با افزودن اسید سولفوریک غلیظ (93%) در یک سری از راکتورهای به خوبی هم زده تولید می شود. این منجر به تولید اسید فسفریک و سولفات کلسیم (گچ) و سایر ناخالصی های نامحلول می شود. سپس آب اضافه می شود و گچ با فیلتراسیون همراه با سایر مواد نامحلول (مانند سیلیس) حذف می شود. فلوراید، به عنوان H2SiF6، در مرحله بعدی با تبخیر حذف می شود.
اگرچه واکنش در مراحلی انجام می شود که شامل دی هیدروژن فسفات کلسیم است، واکنش کلی را می توان به صورت زیر نشان داد:
با این حال، واکنش های جانبی وجود دارد. به عنوان مثال با فلوراید کلسیم و کربنات کلسیم موجود در سنگ:
فلوئوروسیلیسیلیک اسید یک محصول جانبی مهم از این و از ساخت هیدروژن فلوراید است. می توان آن را با هیدروکسید سدیم خنثی کرد تا هگزافلوئوروسیلیکات سدیم را تشکیل دهد. این اسید همچنین برای ساخت فلوراید آلومینیوم استفاده می شود که به نوبه خود در ساخت آلومینیوم استفاده می شود.
ساختار کریستالی سولفات کلسیم تشکیل شده به شرایط واکنش بستگی دارد. در دمای 340-350 کلوین، محصول اصلی دی هیدرات، CaSO4.2H2O است. در دمای 360-380 کلوین، همی هیدرات، CaSO4.1/2H2O تولید می شود.
سولفات کلسیم فیلتر شده و اسید با استفاده از تقطیر خلاء به حدود 56% P2O5 تغلیظ می شود. محصول حاصل از اسید “فرایند مرطوب” ناخالص است اما می تواند بدون خالص سازی بیشتر برای تولید کود مورد استفاده قرار گیرد .
همچنین می توان آن را تا حدود 70% P2O5 تبخیر کرد، محلولی به نام اسید سوپر فسفریک که مستقیماً به عنوان کود مایع استفاده می شود. برای ساخت فسفاتهای صنعتی، اسید با استخراج با حلال با استفاده از متیل ایزوبوتیل کتون (MIBK) خالص میشود که در آن اسید کمی محلول و غلیظ میشود تا محتوای P2O5 60 درصد به دست آید.
این اسید را میتوان با استفاده از حلالها برای استخراج آن از فلزات سنگین و فلوئور زدایی (از طریق تبخیر) برای تولید محصولی با کیفیت غذایی خالصتر کرد.
(ب) فرآیند حرارتی
مواد اولیه برای این فرآیند فسفر و هوا است:
در ابتدا فسفر به داخل کوره پاشیده می شود و در هوا در حدود 1800-3000 کلوین می سوزد.
بیشتر فرآیندها از هوای خشک نشده استفاده می کنند و بسیاری از آنها شامل اضافه کردن بخار به مشعل فسفر برای تولید و نگهداری فیلمی از اسیدهای پلی فسفریک متراکم می شود که از برج مشعل فولاد ضد زنگ (خنک شده با آب خارجی) محافظت می کند. محصولات حاصل از برج مشعل مستقیماً به یک برج هیدراتاسیون منتقل می شوند که در آن اکسید فسفر گازی در اسید فسفریک بازیافتی جذب می شود:
از طرف دیگر، فسفر ممکن است در هوای خشک سوزانده شود. پنتوکسید فسفر به صورت پودر سفید متراکم شده و به طور جداگانه به اسید فسفریک هیدراته می شود.
این روش امکان بازیابی و استفاده مجدد از گرما را فراهم می کند.
سوختن و هیدراتاسیون مستقیم، همانطور که قبلاً توضیح داده شد، شرایط بسیار خورنده را ایجاد می کند. این تجهیزات از فولاد ضد زنگ ساخته شده اند یا با آجر کربنی ساخته شده اند. برای کاهش خوردگی، دیواره های مشعل و برج های هیدراتور خنک می شوند، اما محصولات راکتور در دمای بسیار پایین برای بازیابی گرمای مفید ظاهر می شوند.
اسید محصول دارای غلظت حدود 85٪ است.
اسید تترا فسفریک، یکی از خانواده اسیدهای پلی فسفریک است که می تواند به طور انتخابی تولید شود، یا با جوشاندن آب در دمای بالا در یک ظرف کربنی یا با افزودن پنتوکسید فسفر جامد به اسید فسفریک تقریباً در حال جوش، ساخته می شود. روش اول معمولاً محصول خالص تری را به دلیل محتوای آرسنیک بالای پنتوکسید فسفر ارائه می دهد.
فسفات ها

نمک های اسید فسفریک، فسفات ها، ترکیباتی هستند که به طور گسترده در کشاورزی، صنعت و در خانه استفاده می شود.
الف) فسفات آمونیوم
مونو آمونیوم دی هیدروژن فسفات و دی آمونیوم هیدروژن فسفات به عنوان کود استفاده می شود و از مخلوط کردن نسبت های صحیح اسید فسفریک با آمونیاک بی آب در یک درام چرخان ساخته می شود.
انتخاب اینکه کدام آمونیوم فسفات استفاده شود به نسبت نیتروژن و فسفر مورد نیاز برای محصول بستگی دارد.
ب) فسفات کلسیم
فسفات کلسیم به طور گسترده به عنوان کود استفاده می شود. دی هیدروژن فسفات کلسیم، Ca(H2PO4)2، از واکنش سنگ فسفات با اسید سولفوریک تولید می شود:
این به عنوان سوپر فسفات شناخته می شود. حاوی حدود 20٪ P2O5 است.
اگر سنگ فسفات به جای اسید سولفوریک با اسید فسفریک درمان شود، فرم غلیظ تری از دی هیدروژن فسفات کلسیم با سطح کلی P2O5 بالاتر (50%) تولید می شود:
این به عنوان سوپر فسفات سه گانه شناخته می شود. سطح بالاتر فسفات به این دلیل حاصل می شود که محصول دیگر با سولفات کلسیم رقیق نمی شود.
ج) فسفات سدیم
فسفات سدیم از واکنش اسید فسفریک و محلول غلیظ هیدروکسید سدیم در نسبت های مناسب (استوکیومتری) تولید می شود. محصول متبلور می شود.
مونو سدیم دی هیدروژن فسفات (MSP, NaH2PO4) در فرمولاسیون های تمیز کردن فلزات و آماده سازی سطوح، به عنوان منبع فسفات در تولید دارو، و به عنوان یک عامل کنترل کننده pH در خمیردندان، در پوشش مینای شیشه ای (لوازم بهداشتی) و در ساخت نشاسته فسفات استفاده می شود.
یکی از بزرگترین کاربردها به عنوان یک تصفیه آب حلال در آب آشامیدنی است. برای جلوگیری از انحلال سرب توسط اسیدهای موجود در آب، می توان از اسید فسفریک یا MSP برای تولید یک پوشش نازک نامحلول از فسفات سرب روی لوله های سرب استفاده کرد.
دی سدیم هیدروژن فسفات (Na2HPO4) به عنوان یک عامل نرم کننده در پنیر فرآوری شده، در لعاب ها و لعاب های سرامیکی، در دباغی چرم، در تولید رنگ و به عنوان یک بازدارنده خوردگی در تصفیه آب استفاده می شود.
تری سدیم فسفات (Na3PO4) در پاک کننده های سنگین، به عنوان مثال در چربی زدایی فولاد استفاده می شود. این ماده قلیایی و جداکننده یون های کلسیم است و آنها را در محلول نگه می دارد و از تشکیل تفاله جلوگیری می کند.
دی سدیم پیروفسفات (Na2H2P2O7) به عنوان یک عامل خمیر کننده در نان / کیک استفاده می شود (به آزادسازی دی اکسید کربن از جوش شیرین کمک می کند)، و همچنین به عنوان یک سرکوب کننده اکسید آهن (اثر تیره شدن یا قهوه ای شدن) در ساخت غذاهای مختلف و به عنوان پخش کننده در گل حفاری چاه نفت نیز استفاده میشود.
اسید فسفریک را از کجا بخریم؟
شرکت علمی سازان زینو با برند پک هاوس مفتخر است که اسید فسفریک خوراکی و اسید فسفریک صنعتی را با کیفیت درجه یک و قیمت عالی و ویژه خدمت شما عزیزان ارايه دهد.
بنابراین جهت خرید این ماده و تحویل در اسرع وقت, با کارشناسان ما به شماره های ۰۲۱۸۶۰۵۳۱۷۵ – ۰۲۱۸۸۰۶۹۶۵۸ – ۰۲۱۸۶۰۵۸۹۱۳ تماس بگیرید.
سایر مقالات پربازدید :
| سولفوریک اسید اولئوم چیست ؟ |
حلال ویژه یا وایت اسپریت چیست ؟ | اسید فرمیک زنبورداری | اتیلن گلیکول مونو استئارات چیست؟ | از مونو اتانول آمین چه میدانید ؟ |
| تیتان آناتاز ( آناتاس ) و معرفی این ماده | با فواید و خواص اسید سیتریک برای پوست بیشتر آشنا شوید | اسید نیتریک و طلا | از پیل سوختی متانولی چه میدانید ؟ | معرفی کامل اسید انیدرید |
| ۳ روش مهم تهیه و تولید استون | معرفی کامل اسید سولفوریک | استون و همه اطلاعات از این ماده | اسید نیتریک و اطلاعات جامعی از این ماده شیمیایی | اسید استیک و همه اطلاعات از این ماده |
| مواد شیمیایی و همه چیز در مورد آن | اسید سیتریک و همه اطلاعات از این ماده شیمیایی | تیلوز و همه موارد در مورد این ماده ی شیمیایی | نقش اسید فسفریک در پسته | اسید فسفریک در نوشابه و خطرات آن |
| نرمال بوتانول و همه چیز درمورد این ماده شیمیایی | مشخصات و کاربردهای تولوئن | متیلال ( دی متوکسی متان – DMM ) یا استون ایرانی چیست ؟ | معرفی کامل پرکلرواتیلن و کاربردهای این ماده | مونومر استایرن چیست؟ کاربردها, ایمنی , مراحل تولید و فواید |
منابع:
https://www.essentialchemicalindustry.org
| https://bit.ly/3nYtzUP | https://b2n.ir/j22674 | https://cutt.ly/YT0lmCK |
| yun.ir/qssrh | shorturl.at/iloFJ | https://tinyurl.com/y9vudf66 |









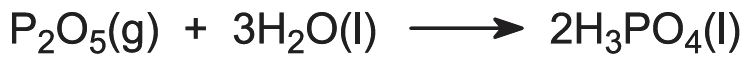

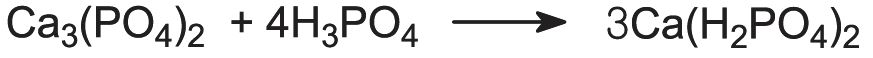
سلام و خسته نباشید
مطالب کاملی در مورد پودر اسید فسفریک بیان کردید سپاس از شما
سلام بر شما
خوشحالیم برایتان مفید بوده است
موفق باشید
سلام و درود
احترام قصد خرید اسید فسفریک خوراکی رو دارم و اطلاعات بیشتری در مورد این ماده میخواستم
سلام بر شما
اطلاعات بیشتر از اسید فسفریک خوراکی: https://packhouse.ir/product/phosphoric-acid/