- 17 آذر 1400
- بدون نظر
اسید سولفوریک چیست ؟
List of Contents
اسید سولفوریک چه نوع اسیدی است ؟
اسید سولفوریک ( در لفظ انگلیسی : sulfuric acid )، با فرمول H 2 S O 4 ، یک اسید معدنی قوی است. در تمام غلظت ها در آب حل می شود. زمانی به روغن ویتریول معروف بود که توسط کیمیاگر قرن هشتم، جابر بن حیان، کاشف احتمالی این ماده شیمیایی ابداع شد .
اسید سولفوریک کاربردهای فراوانی دارد و به جز آب در مقادیر بیشتری نسبت به سایر مواد شیمیایی تولید می شود . تولید جهانی در سال 2001 165 میلیون تن با ارزش تقریبی 8 میلیارد دلار بود.
کاربردهای اصلی شامل فرآوری سنگ معدن، تولید کود ، پالایش نفت،فرآوری فاضلاب و سنتز شیمیایی می باشد. بسیاری از پروتئینها از اسیدهای آمینه حاوی گوگرد (مانند سیستئین و متیونین) ساخته شدهاند که هنگام متابولیزه شدن توسط بدن، این اسید را تولید میکنند.
جرم مولی اسید سولفوریک ۹۸٫۰۷۹ گرم بر مول می باشد.
کاربرد اسید سولفوریک
کاربرد عمده اسید سولفوریک در تولید کودهایی مانند سوپر فسفات آهک و سولفات آمونیوم است. به طور گسترده در ساخت مواد شیمیایی، به عنوان مثال، در ساخت اسید هیدروکلریک، اسید نیتریک، نمک های سولفات، مواد شوینده مصنوعی، رنگ ها و رنگدانه ها، مواد منفجره و داروها استفاده می شود.
کاربرد اسید سولفوریک در شوینده
یک شوینده سدیم آلکیل سولفات را می توان با تصفیه یک الکل با زنجیره بلند با این اسید و خنثی کردن استر حاصل با هیدروکسید سدیم تهیه کرد.رایج ترین شوینده های خانگی سولفونات ها هستند، نمک های بنزن سولفونیک اسیدها که با یک گروه آلکیل با زنجیره بلند جایگزین شده اند.
اسید سولفوریک در کشاورزی
حدود نیمی از اسید سولفوریک جهان در کشاورزی، به ویژه در صنعت کودهای شیمیایی استفاده می شود. این اسید به طور خاص برای تولید کودهای فسفاته مانند سوپر فسفات آهک و سولفات آمونیوم استفاده می شود.
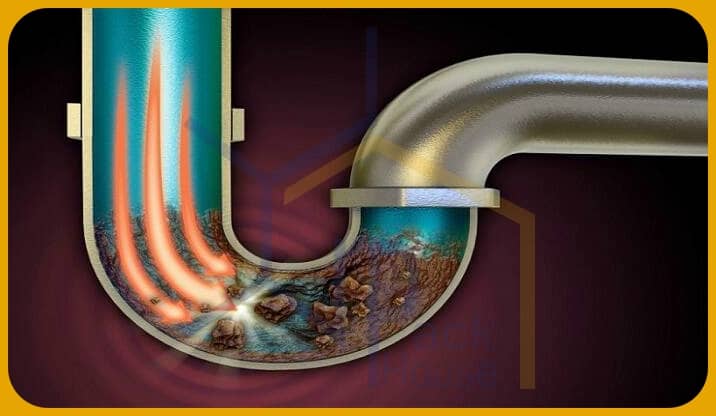
اسید سولفوریک لوله بازکن
اسیدها دسته سوم مواد شیمیایی جهت گرفتگی لوله هستند و بهترین اسیدها برای تمیز کردن لوله های لوله کشی شامل اسید هیدروکلریک و اسید سولفوریک می باشند. پاک کننده های تخلیه اسیدی باید آخرین راه حل باشند و فقط زمانی استفاده شوند که سایر مواد شیمیایی تمیز کننده فاضلاب به اندازه کافی سریع کار نکنند یا نتوانند کار را انجام دهند.
اسید ها خطرناک هستند و به ویژه برای لوله ها یا محیط زیست خوب نیستند، و برخی از کشورها، مانند بریتانیا، استفاده از آنها را توسط افراد دیگری غیر از متخصصان دارای مجوز ممنوع می کنند.
در ایالات متحده، می توانید پاک کننده تخلیه اسید سولفوریک را در فروشگاه های بزرگ با نام های تجاری مانند Kleen-Out، Clean Shot و Liquid Lightning خریداری کنید. اینها محلولهای اسید سولفوریک 93 تا 95 درصد هستند، به این معنی که غلظت بالایی دارند، بنابراین باید با احتیاط با آنها کار کنید. دستورالعمل های روی برچسب محصول را به دقت دنبال کنید و اقدامات احتیاطی استاندارد برای دست زدن به اسید را رعایت کنید.
دستورالعمل های ایمنی برای استفاده از پاک کننده تخلیه اسید سولفوریک
اولین چیزی که در هر کلاس شیمی یاد می گیرید این است که هرگز آب را در اسید نریزید. اگر مجبورید اسید را رقیق کنید، آن را در آب بریزید – هرگز برعکس عمل نکنید . دلیل آن این است که واکنش هیدراتاسیون اسید سولفوریک بسیار گرمازا است، به این معنی که گرما را آزاد می کند و مخلوط می تواند خود به خود بجوشد. اسید از آب متراکم تر است، بنابراین غرق می شود و حباب های انفجاری محلول اسید را در همه جهات می پاشند.
پتانسیل برای اسپری اسید به آب وجود دارد، بنابراین هنگام استفاده از یک پاک کننده تخلیه اسید سولفوریک، شما باید با لباس و عینک محافظ از اجزای بدن خود حفاظت کنید . قبل از استفاده از تمیز کننده تخلیه، اطراف سینک را پاک کنید و شیر آب را بپوشانید زیرا مخلوط خورنده می تواند به هر فلزی که با آن در تماس است آسیب برساند. دستورالعملها توصیه میکنند که مجموعه تخلیه و سایر قسمتهای فلزی سینک را با ژل نفتی بپوشانید.
از آنجایی که این اسید فلز را میخورد ، می تواند به لوله های لوله کشی کروم، فولاد ضد زنگ و فولاد گالوانیزه آسیب برساند. بنابراین توصیه می شود استفاده از تنها اگر شما لوله کشی لوله های پلاستیکی ، و حتی این می تواند باعث آسیب حرارتی حفظ اگر شما معرفی پاک کننده تخلیه بیش از حد سرعت و یا استفاده از بیش از حد از آن است. محصول را به آرامی در آبکش بریزید و فقط از مقدار توصیه شده روی برچسب استفاده کنید.
چه زمانی یک پاک کننده تخلیه اسید سولفوریک را انتخاب کنید
این اسید از طریق تعدادی از مواد مسدود کننده زهکشی می خورد که سایر پاک کننده های فاضلاب، از جمله آنهایی که حاوی هیدروکسید سدیم هستند، این مواد را نمی خورند. این مواد شامل کاغذ، گریس و مو هستند که مواد اصلی تشکیل دهنده بسیاری از گرفتگی های فاضلاب هستند.
اگر لوله های شما به کندی تخلیه می شوند، استفاده از پاک کننده آنزیمی ایمن تر است و اجازه دهید وضعیت به آرامی بهبود یابد، اما اگر لوله ها به طور کامل مسدود شده اند و نمی توانید از سینک استفاده کنید، اسید سولفوریک می تواند سریعا گرفتگی را برطرف کند .
اگر یک پیستون دارید، ممکن است بتوانید گرفتگی را بدون استفاده از مواد شیمیایی پاک کنید، که ایمن ترین گزینه در بین همه گزینه ها است. با این حال، اگر قصد دارید غوطه ور شود، این کار را قبل از استفاده از اسید سولفوریک انجام دهید و هرگز بعد از آن انجام ندهید . به یاد داشته باشید که پاک کننده , تخلیه گرما تولید می کند و ریزش مخلوط داغ در لوله ها یک دستور العمل برای فاجعه است تا جایی که به لوله ها مربوط می شود.
” اسید سولفوریک ” ، مانند عوامل پاک کننده سوز آور مانند هیدروکسید سدیم، برای سیستم های سپتیک ایمن نیست. باکتری های مفید موجود در مخزن را از بین می برد و توانایی سیستم را در هضم زباله ها کاهش می دهد. تنها در صورتی از اسید سولفوریک استفاده کنید که خانه شما به سیستم فاضلاب شهری متصل است.
نحوه استفاده از اسید سولفوریک برای تمیز کردن زهکشی
زمان استفاده از این اسید زمانی است که تمام تلاش ها برای پاکسازی مکانیکی زهکشی، از جمله فرورفتن و ، شکست خورده است. اگر اخیراً از یک ماده شیمیایی تمیز کننده زهکشی دیگر استفاده کرده اید از اسید سولفوریک استفاده نکنید زیرا این مواد شیمیایی می توانند برای ایجاد بخارات سمی ترکیب شوند.
پس از پوشیدن لباس های محافظ، پوشاندن قسمت های آسیب پذیر سینک و زهکشی و خواندن دستورالعمل های کاربرد روی برچسب محصول، از روش زیر استفاده کنید:
- پنجره ها را برای تامین تهویه باز کنید.
- مقدار توصیه شده پاک کننده تخلیه (حدود 200 میلی لیتر یا حدود 7 اونس) را به آرامی در زهکش بریزید.
- حدود 10 ثانیه صبر کنید، سپس شیر آب را باز کنید و اجازه دهید آب به آرامی به داخل فاضلاب برود. اگر زهکشی برگشت، آب را ببندید و کمی بیشتر صبر کنید.
- اگر گرفتگی پاک نشد، اسید بیشتری در زهکش بریزید – تا 500 میلی لیتر یا حدود 16 اونس. حتی بیشتر صبر کنید – چند دقیقه تا یک ساعت – به اسید زمان بدهید تا کار کند.
- وقتی گرفتگی پاک شد و زهکش شروع به جاری شدن کرد، زهکش را با آب فراوان بشویید.
- با مخلوط کردن محلولی از 1/4 فنجان جوش شیرین در هر لیتر آب و ریختن آن در فاضلاب، اسید را خنثی کنید. شما می توانید از این محلول برای خنثی کردن هرگونه ریزش استفاده کنید.
استفاده از اسید سولفوریک برای گرفتگی توالت
ایمن ترین، ساده ترین و موثرترین راه برای پاک کردن گرفتگی توالت استفاده از پیستون است. وقتی این کار نمی کند، می توانید مطمئن شوید که گرفتگی بسیار زیاد است. اسید سولفوریک به اندازهای قوی است که از طریق گرفتگیهای بزرگ خورده شود، اما معمولاً برای توالتها توصیه نمیشود، مخصوصاً اگر خانه دارای سیستم سپتیک باشد. با این حال، حداقل یک پاک کننده تخلیه اسید سولفوریک وجود دارد که برای سیستم های سپتیک ایمن است.
لوله بازکن مایع لایتنینگ یک محلول اسید سولفوریک بافر است که رسوب را تمیز کرده و گرفتگی لوله ها را حل می کند. این به طور گسترده در دسترس است و حدود 10 دلار برای یک ظرف 32 اونس قیمت دارد. اگرچه برای لوله های چدنی یا فولادی گالوانیزه ایمن نیست، بنابراین اگر لوله کشی قدیمی دارید بهتر است از آن استفاده نکنید.
برای استفاده از آن، بین 12 تا 16 اونس، و نه بیشتر، به آرامی در آب توالت بریزید، مراقب باشید که آن را روی زمین یا جای دیگری نپاشید. سپس، 15 دقیقه صبر کنید. پس از پایان دوره انتظار، درب توالت را ببندید و سه بار توالت را شستشو دهید. از طرف دیگر، 3 تا 4 گالن آب سرد را مستقیماً با استفاده از یک سطل داخل کاسه بریزید.
اسید سولفوریک در گلخانه
آیا گیاهان می توانند مستقیماً از اسید سولفوریک استفاده کنند؟
در توضیح چرخه گوگرد اغلب گفته می شود که گوگرد به صورت اسید سولفوریک توسط باران اسیدی از جو به سمت زمین حرکت می کند. آیا گیاهان می توانند مستقیماً از اسید سولفوریک برای جذب گوگرد استفاده کنند؟
گیاهان دارای ناقل سولفات هستند که از آنها برای جذب گوگرد استفاده می کنند. از آنجایی که سولفات پایه مزدوج اسید سولفوریک است، این می تواند به عنوان “بله” برای سوال شما تعبیر شود. این اسید به شکل باز مزدوج خود در مقادیر PH فیزیولوژیکی وجود دارد.
با این حال، عاقلانه نیست که گیاهان خود را با اسید سولفوریک آبیاری کنید، زیرا بسیاری از گیاهان دارای محدوده pH بهینه هستند که زمانی که اسید سولفوریک pH خاک را زیر آن محدوده کاهش دهد، به سرعت باعث مرگ می شود. در نتیجه، مناطق آسیب دیده توسط باران اسیدی ممکن است برای حل این مشکل نیاز به درمان با سنگ آهک قلیایی داشته باشند .
اسید سولفوریک برای سیب زمینی
کشاورزان سیب زمینی قبل از برداشت، مزارع سیب زمینی خود را با محلول اسید سولفوریک اسپری می کنند تا در طی یک یا دو روز، قسمت های سبز از بین رفته و سیاه شوند. این به خشک شدن ساقه کمک می کند و از گره خوردن آنها در تجهیزات برداشت جلوگیری می کند.
تاریخچه اسید سولفوریک
کشف اسید سولفوریک را به جابر بن حیان کیمیاگر قرن هشتم نسبت می دهند . بعداً توسط پزشک و کیمیاگر قرن نهم، ابن زکریای رازی (راسس)، که این ماده را با تقطیر خشک مواد معدنی از جمله هپتاهیدرات سولفات آهن (II)، FeSO 4 • 7H 2 O، و سولفات مس (II) به دست آورد، مورد مطالعه قرار گرفت.
پنتا هیدرات، CuSO 4 • 5H 2 O. هنگامی که حرارت داده می شود، این ترکیبات به ترتیب به اکسید آهن (II) و اکسید مس (II) تجزیه می شوند و آب می دهند وتری اکسید گوگرد، که ترکیب شده و محلول رقیق اسید سولفوریک تولید می کند. این روش از طریق ترجمه رساله ها و کتاب های عربی و فارسی توسط کیمیاگران اروپایی مانند آلبرتوس مگنوس آلمانی قرن سیزدهم در اروپا رایج شد .
اسید سولفوریک در میان کیمیاگران اروپایی قرون وسطی به عنوان روغن ویتریول شناخته میشد. کلمه ویتریول از کلمه لاتین vitreus به معنای شیشه به معنای ظاهر شیشه ای نمک های سولفات است که نام ویتریول را نیز یدک می کشد. نمک هایی که به این نام خوانده می شوند شامل سولفات مس (II) (ویتریول آبی یا به ندرت ویتریول رومی)، سولفات روی (ویتریول سفید)، سولفات آهن (II) (ویتریول سبز)، سولفات آهن (III) (ویتریول مریخ) و سولفات کبالت (II) (ویتریول قرمز) میباشند.
ویتریول به طور گسترده ای مهمترین ماده کیمیاگری در نظر گرفته می شد که برای استفاده به عنوان سنگ فلسفی در نظر گرفته شد . ویتریول با خالصسازی بالا بهعنوان محیطی برای واکنش دادن به مواد مورد استفاده قرار گرفت.
این عمدتاً به این دلیل بود که اسید با طلا که اغلب هدف نهایی فرآیندهای کیمیاگری است، واکنش نشان نمیدهد . اهمیت ویتریول برای کیمیاگری در شعار کیمیاگری Visita Interiora Terrae Rectificando Invenies Occultum Lapidem (“از داخل زمین بازدید کنید و با اصلاح (یعنی پاکسازی) سنگ پنهان/مخفی را خواهید یافت”) برجسته شده است. در L’Azoth des. فیلسوفهای کیمیاگر قرن پانزدهم باسیلیوس والنتینوس، که مخفف آن است .
در قرن هفدهم، یوهان گلابر، شیمیدان آلمانی-هلندی، اسید سولفوریک را با سوزاندن گوگرد همراه با نمک (نیترات پتاسیم ، KNO 3 ) در حضور بخار تهیه کرد. با تجزیه نمک نمک، گوگرد را به SO 3 اکسید می کند که با آب ترکیب می شود و اسید سولفوریک تولید می کند. در سال 1736، جاشوا وارد، داروساز لندنی ، از این روش برای شروع اولین تولید این اسید در مقیاس بزرگ استفاده کرد.
در سال 1746 در بیرمنگام ، جان روباک شروع به تولید اسید سولفوریک از این طریق در محفظههای سربی کرد ، محفظههایی که قویتر، ارزانتر بودند و میتوانستند بزرگتر از ظروف شیشهای که قبلاً استفاده میشد ساخته شوند. این فرآیند محفظه سرب امکان صنعتی سازی موثر تولید اسید سولفوریک را فراهم کرد و با اصلاحات متعدد تقریباً برای دو قرن روش استاندارد تولید باقی ماند.
اسید سولفوریک جان روباک تنها حدود 35 تا 40 درصد اسید بود. اصلاحات بعدی در فرآیند محفظه سرب توسط شیمیدان فرانسوی ژوزف-لوئیس گی-لوساک و شیمیدان انگلیسی جان گلاور این میزان را به 78% ارتقا داد.
با این حال، ساخت برخی از رنگها و سایر فرآیندهای شیمیایی نیاز به محصول غلیظتری دارد و در طول قرن هجدهم، این امر تنها با تقطیر خشک مواد معدنی با روشی مشابه فرآیندهای اولیه کیمیاگری امکانپذیر بود .
پیریت ( دی سولفید آهن، FeS است 2 ) در هوا به عملکرد گرم شده بود آهن (II) سولفات، FeSO 4 ، که با حرارت دادن بیشتر در هوا به شکل اکسید شده بود آهن (III) سولفات، آهن 2(SO 4 ) 3 که وقتی تا دمای 480 درجه سانتیگراد گرم می شود به اکسید آهن (III) و تری اکسید گوگرد تجزیه می شود که می تواند از آب عبور داده شود تا اسید سولفوریک در هر غلظتی تولید شود. هزینه این فرآیند از استفاده در مقیاس بزرگ از اسید سولفوریک غلیظ جلوگیری کرد.
در سال 1831، تاجر بریتانیایی سرکه، Peregrine Phillips، یک فرآیند بسیار مقرونبهصرفهتر را برای تولید تریاکسید گوگرد و اسید سولفوریک غلیظ، که امروزه به عنوان فرآیند تماس شناخته میشود، به ثبت رساند . اساساً تمام عرضه اسید سولفوریک جهان اکنون با این روش تولید می شود.
اسید سولفوریک فرازمینی
اسید سولفوریک در اتمسفر فوقانی زهره توسط اثر فتوشیمیایی خورشید بر روی دی اکسید کربن ، دی اکسید گوگرد و بخار آب تولید می شود. فوتون های فرابنفش با طول موج های کمتر از 169 نانومتر می توانند دی اکسید کربن را به مونوکسید کربن و اکسیژن اتمی تبدیل کنند .
اکسیژن اتمی بسیار واکنش پذیر است. هنگامی که با دی اکسید گوگرد، یک جزء ناچیز جو زهره، واکنش نشان می دهد، نتیجه تری اکسید گوگرد است که می تواند با بخار آب، یکی دیگر از اجزای کمیاب جو زهره، ترکیب شود و اسید سولفوریک تولید کند.
CO 2 → CO + O
SO 2 + O → SO 3
SO 3 + H 2 O → H 2 SO 4
در بخشهای فوقانی و خنکتر جو زهره، اسید سولفوریک میتواند به صورت مایع وجود داشته باشد و ابرهای غلیظ اسید سولفوریک سطح سیاره را از بالا کاملاً پنهان میکنند. لایه ابر اصلی از 45 تا 70 کیلومتری سطح سیاره گسترش یافته است، با مه های نازک تر که تا ارتفاع 30 کیلومتری و 90 کیلومتری بالای سطح گسترش می یابد.
طیفهای فروسرخ از مأموریت گالیله ناسا، جذبهای مشخصی را در اروپا، قمر مشتری ، نشان میدهد که به یک یا چند هیدرات اسید سولفوریک نسبت داده شده است. تفسیر طیف ها تا حدودی بحث برانگیز است. برخی از دانشمندان سیارهشناسی ترجیح میدهند که ویژگیهای طیفی را به یون سولفات اختصاص دهند، شاید به عنوان بخشی از یک یا چند ماده معدنی در سطح اروپا.
اسید سولفوریک ۹۸٪
آیا اسید سولفوریک ۹۸ درصد خورنده است؟
مقابله با اسید سولفوریک دشوار است زیرا خواص خورندگی آن با سرعت، غلظت، ناخالصی ها و دما به طور چشمگیری تغییر می کند. جالب توجه است که اسید سولفوریک ۹۸ درصد کمتر از ۹۳ درصد خورنده است و هر دو نسبت به غلظت اسید سولفوریک متوسط خورنده کمتری هستند.
غلظت اسید سولفوریک ۹۸٪ چقدر است؟
غلظت اسید سولفوریک ۹۸درصد , ۱.۸۴ می باشد.
رقت ها برای ساخت محلول 1 مولار :
| معرفهای غلیظ | چگالی | مولاریتی |
| اسید پرکلریک ۷۰٪ | ۱.۶۷ | ۱۱.۶ |
| اسید اورتوفسفریک ۸۵٪ | ۱.۷ | ۱۵.۲ |
| سدیم هیدروکسید ۴۷٪ | ۱.۵ | ۱۷.۶ |
| سولفوریک اسید ۹۸٪ | ۱.۸۴ | ۱۸.۴ |
اسید سولفوریک را از کجا بخریم؟
شرکت علمی سازان زینو با برند پک هاوس مفتخر است که این ماده را با کیفیت درجه یک و قیمت عالی و ویژه خدمت شما عزیزان ارايه دهد.
بنابراین جهت خرید اسید سولفوریک و تحویل در اسرع وقت, با کارشناسان ما به شماره های ۰۲۱۸۶۰۵۳۱۷۵ – ۰۲۱۸۸۰۶۹۶۵۸ – ۰۲۱۸۶۰۵۸۹۱۳ تماس بگیرید.
سایر مقالات پربازدید :
معرفی اسیدهای پرکاربرد و ۱۰ اسید رایج و کاربردی
از مونو اتانول آمین چه میدانید ؟
اتیلن گلیکول مونو استئارات چیست؟
اسید اگزالیک و معرفی این ماده
حلال ویژه یا وایت اسپریت چیست ؟
سولفوریک اسید اولئوم چیست ؟
تیتان آناتاز ( آناتاس ) و معرفی این ماده
اسید فسفریک در نوشابه و خطرات آن
با فواید و خواص اسید سیتریک برای پوست بیشتر آشنا شوید
از پیل سوختی متانولی چه میدانید ؟
معرفی کامل اسید انیدرید
۳ روش مهم تهیه و تولید استون
استون و همه اطلاعات از این ماده
اسید نیتریک / کاربردها , روش ساخت و خطرات
اسید فسفریک و همه چیز در مورد این ماده شیمیایی
اسید استیک و همه اطلاعات از این ماده
مواد شیمیایی و همه چیز در مورد آن
اسید سیتریک و همه اطلاعات از این ماده شیمیایی
تیلوز و همه موارد در مورد این ماده ی شیمیایی
نرمال بوتانول و همه چیز درمورد این ماده شیمیایی
مشخصات و کاربردهای تولوئن
متیلال ( دی متوکسی متان – DMM ) یا استون ایرانی چیست ؟
مونومر استایرن چیست؟ کاربردها, ایمنی , مراحل تولید و فواید
منابع:
https://biology.stackexchange.com
| https://bit.ly/3y3onT3 | https://b2n.ir/y31087 | https://cutt.ly/zYx6WiJ |
| yun.ir/q3j89e | shorturl.at/cpwSW | https://tinyurl.com/y5wp9uy4 |